我们心爱的电脑中最重要组成部分——各种芯片的核心是以硅元素为基础晶圆制造的,硅甚至被誉为“电之元素”,由此可见硅对电子工业的重要性。硅元素是世界上储量最丰富的元素之一,然而它对我们来说却是既熟悉又陌生,究竟如何用硅制造出晶圆来的呢?
固有特性
众所周知,硅(旧称矽,英文名称Silicon)是一种非金属元素,位于元素周期表中第4主族,原子序数14,元素符号为Si,它的熔点为1410°C,沸点为2355°C。地壳含有的各元素中硅的含量高达26%,仅次于氧元素,硅常常以沙子或者石英等形式存在于地表及岩石中。对于芯片制造业和太阳能电池工业来说,都需要极高纯度的硅,而我们能从上述各种矿石(主要成分均为二氧化硅)中提炼出几乎完全纯净的硅。硅看起来就是下图这个样子:

半导体
毫无疑问,硅元素的价值在于它是一种半导体——电导率介于导体和绝缘体之间,并且电导率会随着有无杂质及温度变化而显著变化的一种物质。除了硅之外,锗、硒和氧化锡等均为半导体。半导体有不同的种类,可分为空穴型半导体和电子型半导体,前者通过晶体中的空穴导电,后者和金属一样通过电子导电。
单晶硅的生产
(1)硅的主要来源是石英砂(二氧化硅),硅元素和氧元素通过共价键连接在一起。因此需要将氧元素从二氧化硅中分离出来,换句话说就是要将硅还原出来,采用的方法是将二氧化硅和碳元素(可以用煤、焦炭和木屑等)一起在电弧炉中加热至2100°C左右,这时碳就会将硅还原出来。化学反应方程式为:SiO2 (s) + 2C (s) = Si (s) + 2CO (g)(吸热)
(2)上一步骤中得到的硅中仍有大约2%的杂质,称为冶金级硅,其纯度与半导体工业要求的相差甚远,因此还需要进一步提纯。方法则是在流化床反应器中混合冶金级硅和氯化氢气体,最后得到沸点仅有31°C的三氯化硅。化学反应方程式为:Si (s) + 3HCl (g) = SiHCl3 (g) + H2 (g)(放热)
(3)随后将三氯化硅和氢气的混合物蒸馏后再和加热到1100°C的硅棒一起通过气相沉积反应炉中,从而除去氢气,同时析出固态的硅,击碎后便成为块状多晶硅。这样就可以得到纯度为99.9999999%的硅,换句话说,也就是平均十亿个硅原子中才有一个杂质原子。
(4)进行到目前为止,半导体硅晶体对于芯片制造来说还是太小,因此需要把块状多晶硅放入坩埚内加热到1440°C以再次熔化,如下图所示:

为了防止硅在高温下被氧化,坩埚会被抽成真空并注入惰性气体氩气。之后用纯度99.7%的钨丝悬挂硅晶种探入熔融硅中,晶体成长时,以2~20转/分钟的转速及3~10毫米/分钟的速率缓慢从熔液中拉出:
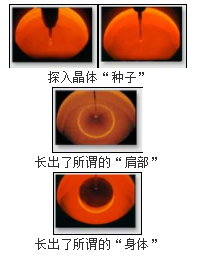
这样一段时间之后就会得到一根纯度极高的硅晶棒,理论上最大直径可达45厘米,最大长度为3米。

以上所简述的硅晶棒制造方法被称为切克劳斯法(Czochralski process,也称为柴氏长晶法),此种方法因成本较低而被广泛采用,除此之外,还有V-布里奇曼法(Vertikalern Bridgman process)和浮动区法(floating zone process)都可以用来制造单晶硅。
芯片成形
上面生产出的硅晶棒首先经过打磨,然后用金刚石锯切成大约1毫米厚的圆片,然后再经过精细打磨、去除瑕疵的若干步骤就得到所谓的晶圆(Wafer),之后就要在晶圆上添入掺杂物以及用蚀刻法分层制造出电路,然后经过分割、打磨、测试等若干步骤,最后将芯片用塑料、陶瓷等材料进行封装并引出镀金引脚,再进行测试等若干步骤,一颗芯片就面世了。
当然,晶圆及芯片生产具体过程中很多细节及步骤并未提及,实际生产过程中远比以上所说的复杂,因此硅晶圆成品率及直径等都是衡量一个国家科技实力的标志之一。